La vita è spesso definita in base a un elenco di proprietà
che distinguono i sistemi viventi da quelli non viventi. Sebbene vi sia una
certa sovrapposizione, questi elenchi sono spesso diversi, a seconda degli
interessi degli autori. Edward Trifonov ha raccolto nel 2011 più di 120 definizioni di vita, cercando un
denominatore comune, ma questo approccio non è sembrato scientifico a molti:
ogni tentativo di definizione è legato a una teoria da cui deriva il suo
significato e non può essere ottenuto da pratiche combinatorie.
Gli esseri viventi condividono una serie di proprietà che non sono presenti contemporaneamente nella materia inanimata, sebbene si possano trovare esempi di materia che esibisce l'una o l’altra, ma mai insieme. Le entità viventi metabolizzano, cioè ricavano energia chimica dalla degradazione di sostanze nutritive ricche di energia, dall’ambiente o dall’energia solare; convertono le molecole nutritive nei precursori di base delle macromolecole cellulari; utilizzano questi precursori per formare altre sostanze organiche con diversa natura e funzioni; formano e degradano biomolecole necessarie a funzioni specializzate delle cellule.
Inoltre,
crescono, si riproducono, interagiscono con il loro ambiente, hanno strutture
organizzate complesse, variabilità ereditabile e hanno discendenze che possono
evolversi nel tempo, producendo strutture funzionali nuove che forniscono una
maggiore capacità di adattamento in ambienti mutevoli. La riproduzione
coinvolge non solo la replicazione degli acidi nucleici che trasportano
l'informazione genetica, ma anche la costruzione epigenetica dell'organismo
attraverso meccanismi di metilazione di acidi nucleici e proteine che
non coinvolgono il genotipo.
Ciò che è vivo ha strutture organizzate e complesse che
svolgono queste funzioni, oltre a percepire e rispondere agli stati interni e
all'ambiente esterno e impegnarsi nel movimento all'interno di quell'ambiente.
Va ricordato che i fenomeni evolutivi sono un aspetto inestricabile dei sistemi
viventi; ogni tentativo di definire la vita in assenza di questa prospettiva
diacronica è vano.
La scuola inglese
Il dibattito moderno sul rapporto tra materia e vita si sviluppò
durante il periodo in cui i biochimici stavano cercando di definire il loro
campo come una disciplina separata dalla chimica o dalla fisiologia, intorno al
1930.
Lo scienziato e divulgatore britannico John B. S. Haldane
in The Sciences and Philosophy (1929) si
oppose alla riduzione dei fenomeni biologici a spiegazioni meccanicistiche,
poiché vedeva la struttura degli organismi biologici e la loro azione diversi
da ciò che si vedeva nei sistemi fisici. Le leggi della chimica e della fisica
non erano abbastanza solide per spiegare la biologia. “È la vita che stiamo
studiando in biologia, e non fenomeni che possono essere rappresentati da
concezioni causali della fisica e della chimica”.
Il biologo sperimentale e statistico medico Lancelot
Hogben, nel libro The Nature of Living Matter (1930), lamentava il
disinteresse di molti biologi del suo tempo per il ruolo dell’ambiente nello
sviluppo degli organismi e sosteneva una visione riduzionista. Per Hogben, la
natura della scienza è che le sue risposte sono sempre incomplete ed essa non
ha gli stessi obiettivi della filosofia. Hogben non vedeva la necessità di
abbandonare la metodologia riduzionista che la biochimica stava
sviluppando.
Per Joseph H. Woodger (Biological Principles: A Critical
Study, 1929) la risoluzione doveva giungere dal
riconoscimento dell'importanza primaria dell'organizzazione biologica e dei
suoi livelli: “per cellula quindi intendo un certo tipo di organizzazione
biologica, non un'entità concreta”. Woodger esortava ad abbandonare l'uso
della parola "vita" nel discorso scientifico sulla base del fatto che
"organismo vivente" era ciò che doveva essere spiegato. Per Woodger
la domanda sul come è nata la vita è al di fuori della scienza.
Forse il luogo in cui il problema della natura della vita
venne affrontato con maggiore insistenza fu il Dipartimento di Biochimica
dell'Università di Cambridge. Durante la prima metà del ventesimo secolo, sotto
la guida del biochimico Sir Frederick Gowland Hopkins, il dipartimento stabilì
gran parte del quadro concettuale e della metodologia, oltre a formare molti
dei più noti esponenti del settore. Hopkins credeva che, sebbene gli esseri
viventi non disubbidiscano a nessuna legge fisica o chimica, essi le
sostanziano in modi che richiedono la comprensione dei fenomeni biologici, dei
vincoli e dell'organizzazione funzionale.
Nel suo importante discorso alla British Association for
the Advancement of Science tenuto nel 1913, Hopkins respinse sia il
riduzionismo dei chimici organici che cercavano di dedurre in vitro ciò
che doveva accadere in vivo, sia il cripto-vitalismo di molti fisiologi
che osservavano il protoplasma delle cellule viventi come vivo in sé stesso e
irriducibile all'analisi chimica. Ciò che Hopkins offriva invece era una
visione della cellula come una macchina chimica, obbediente alle leggi della
termodinamica e della chimica fisica in generale, ma con strutture e funzioni
molecolari organizzate. La cellula vivente “non è un grumo di materia
composto da un gruppo di molecole simili, ma un sistema altamente
differenziato: la cellula, nella moderna concezione della chimica fisica, è un
sistema di fasi coesistenti di diversa natura”. Capire come si era
realizzata l'organizzazione era tanto importante quanto sapere come si erano
verificate le reazioni chimiche. Per Hopkins la vita è “una proprietà della
cellula nel suo insieme, perché dipende dall'organizzazione dei processi”.
Hopkins era influenzato dalla filosofia di Alfred North Whitehead sviluppata in Process and reality (1929), che
sosteneva che la realtà consiste di processi piuttosto che di oggetti
materiali, e che i processi sono meglio definiti dalle loro relazioni con altri
processi, rifiutando così la teoria secondo cui la realtà è fondamentalmente
costituita da pezzi di materia che esistono indipendentemente l'uno dall'altro.
Un membro del dipartimento di Cambridge, il biochimico,
storico della scienza e più tardi grande sinologo Joseph Needham, si impegnò
attivamente nel divulgare le idee di Hopkins nella comunità intellettuale
scrivendo della base filosofica della biochimica in Science, Religion and
Reality (1925). Needham seguì Hopkins nell'affermare che la questione
cruciale non era più il rapporto tra sostanza vivente e non vivente, ma anche
tra mente e corpo, e la biochimica doveva affidare alla filosofia e alle allora
nascenti neuroscienze quest'ultima questione, affinché potesse concentrarsi sul
conoscere la materia vivente. Un altro membro del dipartimento di biochimica,
Norman Pirie, nel 1937 argomentò che essa non poteva essere adeguatamente definita
da un elenco di qualità e nemmeno di processi, poiché la vita "non può
essere definita in termini di una variabile". Per il programma del
gruppo di Hopkins c’era la sfida di capire come leggi fisiche e chimiche
piuttosto semplici possano produrre la complessità dei sistemi viventi.
Durante gli anni '30 un gruppo informale, noto come Biotheoretical
Gathering, si riuniva a Cambridge e comprendeva diversi membri del
dipartimento di biochimica e un certo numero di altri scienziati di Cambridge e
filosofi. Questo gruppo aveva l'obiettivo di costruire una biologia teorica e
filosofica transdisciplinare, che aiutasse a gettare le basi per l’affermazione
della biologia molecolare. Il programma di ricerca di Hopkins era ben
consolidato e fu collegato al lavoro del Biotheoretical Gathering,
influenzando John B. S. Haldane, che diede importanti contributi alla teoria
degli enzimi e alla creazione della moderna sintesi evolutiva, il neodarwinismo. Haldane avrebbe svolto un ruolo
importante nello spostare la preoccupazione dalla natura della vita alla sua
origine come soggetto di studio scientifico. Haldane sospettava, insieme a
Pirie, che una definizione di vita pienamente soddisfacente fosse impossibile,
ma affermava che la definizione materiale era un obiettivo ragionevole per la
scienza. Vedeva la vita come “un modello di processi chimici. Questo modello
ha proprietà speciali. Genera uno schema simile, come fa una fiamma, ma si
regola come una fiamma non fa”. L'uso della metafora della fiamma per
l'attività metabolica cellulare implicava un processo di non equilibrio in un
sistema aperto in grado di riprodursi, ma anche, al limite della metafora, di
autoregolazione. In ciò, Haldane rifletteva la preoccupazione di capire come la
materia e le leggi fisiche potessero portare a fenomeni biologici.
Cos'è la vita? di
Schrödinger
Nel 1943 il grande fisico Erwin Schrödinger (sì, quello dell'equazione della funzione d'onda e del paradosso del gatto) tenne una serie
di conferenze al Dublin Institute for Advanced Studies, che furono
pubblicate come What is Life? nel 1944. Questo piccolo libro ebbe un
grande impatto sullo sviluppo della biologia del ventesimo secolo, specialmente
sui fondatori della biologia molecolare. Schrödinger si chiedeva come fosse
possibile che ci fosse un ordine duraturo nelle molecole responsabile
dell'ereditarietà, quando era ben noto che gli insiemi statistici di molecole
diventavano rapidamente disordinati (con un aumento dell'entropia come previsto
dalla seconda legge della termodinamica). Il problema dell'ereditarietà fu
quindi riformulato a livello molecolare con la domanda “Come l'ordine può
dar luogo all'ordine?” L'altro argomento principale che interessava
Schrödinger era la termodinamica degli esseri viventi in generale, ovvero “Come
possono generare ordine dal disordine attraverso il loro metabolismo?”
Fu la
risposta alla prima domanda che catturò l'attenzione dei fondatori della nuova
biologia. Schrödinger sosteneva che il materiale molecolare doveva essere un
solido "aperiodico" che aveva incorporato nella sua struttura un
"codice in miniatura". Le idee di “'cristallo aperiodico” e di
“codice” non erano in realtà originali (il DNA era stato scoperto dallo
svizzero Friedrich Miescher nel 1869, ma il suo ruolo nella riproduzione e
la forma elicoidale erano ancora sconosciuti), ma insistevano sull'ipotesi di
una logica molecolare della vita. Ciò voleva dire che la struttura degli atomi
che comprendono la molecola dell’eredità non possedeva un singolo ordine
periodico ripetitivo, ma avrebbe avuto piuttosto un ordine di livello superiore
a causa della struttura delle sue subunità molecolari; era questo ordine di
livello superiore, ma aperiodico, che avrebbe contenuto le informazioni
codificate dell'ereditarietà.
Nel 1952 l'esperimento di Alfred D. Hershey e Martha
Chase provò definitivamente che il materiale genetico è costituito
da DNA e non da proteine. Con la scoperta nel 1953 della struttura a
doppia elica del DNA da parte di James D. Watson e Francis H.C. Crick, la
specificità biologica fu ricondotta alla sequenza definita e unica dei nucleotidi
che trasporta quella che da quel momento viene chiamata l'informazione
genetica. 'Specificità' e 'informazione' vennero a coincidere e nel 1958 Crick
affermava che "la specificità di un pezzo di acido nucleico è espressa
solamente dalla sequenza delle sue basi, e [che tale] sequenza è un
codice (semplice) per la sequenza di amminoacidi di una particolare
proteina"; quindi "informazione significa determinazione
precisa della sequenza, sia delle basi nell'acido nucleico sia dei residui
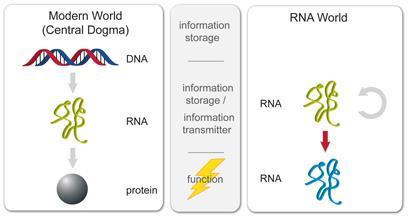
amminoacidici della proteina". Nello stesso anno, Crick definiva
il “dogma centrale” della biologia molecolare, secondo cui il flusso
dell'informazione genetica è monodirezionale: parte dagli acidi nucleici per
arrivare alle proteine, senza considerare un percorso inverso.
La delucidazione della struttura del DNA e la maggior
comprensione della genetica molecolare eclissò l'altra parte dell'argomentazione
di Schrödinger, cioè che l'aspetto più importante del metabolismo è che esso
rappresenta il modo della cellula di affrontare l'entropia che non può fare a
meno di produrre mentre costruisce il suo ordine interno, ciò che Schrödinger
definì "negentropia". Egli notò che la cellula deve mantenersi
in uno stato lontano dall'equilibrio poiché l'equilibrio termodinamico è la
definizione stessa di morte. Creando ordine e organizzazione all'interno di un
sistema vivente (cellule, organismi o ecosistemi), le attività metaboliche
devono produrre un maggiore disordine nell'ambiente, in modo che la seconda
legge non venga violata. Legò le due nozioni, di ordine dall'ordine e ordine
dal disordine, affermando che "il dono sorprendente di un organismo di
concentrare un “flusso di ordine” verso se stesso e sfuggire così al
decadimento nel caos atomico - di “bere ordine” da un ambiente adatto — sembra
essere collegato alla presenza di “solidi aperiodici”, le molecole
cromosomiche, che rappresentano senza dubbio il più alto grado di associazione
atomica ben ordinata che conosciamo (molto più alto del normale cristallo
periodico) in virtù del ruolo individuale che ogni atomo e ogni radicale sta
giocando”.
L’ordine che crea l’ordine
L'impatto del piccolo volume di Schrödinger su una
generazione di fisici e chimici che furono attratti dalla biologia e che
fondarono la biologia molecolare fu duraturo. La conoscenza delle basi
proteiche e degli acidi nucleici dei sistemi viventi continua ad essere
ottenuta a un ritmo accelerato, con il sequenziamento del genoma umano come
punto di riferimento importante lungo il percorso che ha portato all’ingegneria
genetica (tecnologia del DNA ricombinante).
In Il gene egoista (1976, 1989), l’etologo, biologo
e divulgatore Richard Dawkins identificò nel gene, anziché nell'organismo
individuale, il soggetto principale della selezione naturale che conduce il
processo evolutivo. Dawkins, affermava che: “L'unità fondamentale della
selezione, e quindi dell'egoismo, non è né la specie né il gruppo e neppure, in
senso stretto, l'individuo, ma il gene, l'unità dell'ereditarietà”. Nel
descrivere i geni come egoisti, l'autore non intendeva (come è
inequivocabilmente dichiarato nel libro) implicare che sono guidati da motivi o
volontà, ma semplicemente che i loro effetti possono essere accuratamente
descritti come se lo fossero. Il mondo è diviso in replicatori, molecole
stabili che, a differenza delle altre, hanno la capacità di replicarsi, che sono visti come il livello fondamentale di azione per la
selezione naturale, e interattori, le molecole e le strutture codificate
dai replicatori. Questi replicatori si diffusero nel “brodo primordiale”, popolando il mare. Il
processo di replicazione non è però perfettamente fedele, in alcuni casi si
creano delle copie sbagliate. L'errore di copiatura ha giocato un ruolo
fondamentale nell'evoluzione della vita, poiché permise la propagazione di
molecole diverse tra loro, alcune delle quali riuscivano a replicarsi meglio.
La competizione fra queste molecole e le avversità ambientali selezionavano i
replicatori più adatti, i quali perfezionarono le loro tecniche di
propagazione. Alcuni di essi, ipotizzava Dawkins, potrebbero essersi evoluti in
modo da potersi "nutrire" di altri replicatori, altri ancora
potrebbero aver costruito una sorta di scudo di protezione dagli agenti
esterni, dando vita alle prime forme di cellule primordiali. I replicatori di
oggi sono i geni all'interno degli organismi viventi. In effetti, Dawkins
relegava gli organismi allo stato di veicoli genici, o macchine di sopravvivenza.
Le idee di Dawkins suscitarono una reazione a quella che
venne percepita come un'eccessiva enfasi sulla replicazione degli acidi
nucleici. In particolare, i teorici dei sistemi di sviluppo hanno sostenuto un
pluralismo causale nella biologia dello sviluppo e dell'evoluzione. La
posizione di Dawkins fu fortemente contestata dagli americani Niles Eldredge,
paleontologo, e Stephen Jay Gould, biologo, paleontologo e storico della
scienza, estensori della teoria degli equilibri punteggiati. Tale teoria
sostiene che i cambiamenti evolutivi avvengono in periodi di tempo
relativamente brevi (su scala geologica) sotto l'impulso di forze selettive
ambientali; questi periodi di variazione evolutiva sarebbero intervallati da
lunghi periodi di stabilità. L'accesa e prolungata polemica di Gould contro
Dawkins nasceva dalla sua opposizione al determinismo sotteso al suo pensiero,
a favore dell'indeterminismo che, secondo Gould sta alla base della maggior
parte dei processi biologici innovativi. Nella visione di Gould, come peraltro
in quella già del francese Jacques Monod e di tutti i biologi
evoluzionisti, il caso (serie di cause sconnesse o causalità intricata) produce
il nuovo, mentre la necessità, attraverso la selezione naturale che opera in
base a causalità lineare, conserva l'adatto ed elimina l'inadatto.
Un altro oppositore di Dawkins fu il genetista Richard
Lewontin, il quale sosteneva che, mentre il darwinismo tradizionale ha
descritto l'organismo come soggetto passivo di influenze ambientali, sarebbe
più corretto descrivere l'organismo come costruttore attivo del suo ambiente.
Le nicchie ecologiche non sono ricettacoli
precostituiti in cui gli organismi vengono inseriti, ma sono definite e create
dagli organismi stessi. Il rapporto organismo-ambiente è dunque reciproco e
dialettico. Lewontin è stato un critico tenace di alcuni temi del
neodarwinismo; in particolare ha criticato coloro che, come anche Dawkins, tentavano
di spiegare i comportamenti e le strutture sociali degli animali in termini di
vantaggio o di strategia evoluzionistici; questo indirizzo di studio, secondo
Lewontin, può essere considerato come una forma di determinismo genetico.
Il disordine che crea l’ordine
Meno noto è l'oltre mezzo secolo di lavoro ispirato
dall'altro pilastro del discorso di Schrödinger, cioè come gli organismi
ottengono ordine dal disordine attraverso la termodinamica di sistemi aperti
lontani dall'equilibrio. Tra i primi studiosi di tale termodinamica di non
equilibrio spicca il chimico e fisico Ilya Prigogine, noto soprattutto per la
sua definizione di strutture dissipative e il loro ruolo nei sistemi
termodinamici lontani dall'equilibrio, una scoperta che gli è valsa il Premio
Nobel per la Chimica nel 1977. Una struttura dissipativa è un sistema
termodinamicamente aperto che opera in uno stato lontano dall'equilibrio
termodinamico, scambiando con l'ambiente energia, materia e/o entropia. I
sistemi dissipativi sono caratterizzati dalla formazione spontanea di
anisotropia, ossia di strutture ordinate e complesse, a volte caotiche. Questi
sistemi, quando attraversati da flussi crescenti di energia, materia e
informazione, possono anche evolvere e, passando attraverso fasi di
instabilità, aumentare la complessità della propria struttura (ovvero l'ordine)
diminuendo la propria entropia. In sintesi, Ilya Prigogine ha scoperto che l'importazione e
la dissipazione di energia nei sistemi chimici potrebbe risultare
nell'emergenza di nuove strutture (quindi strutture dissipative) dovute
all'auto-organizzazione interna. In natura esistono organismi viventi in grado
di auto-organizzarsi diminuendo la propria entropia a discapito dell'ambiente,
vincolati a un maggior o minor disordine entropico. A partire da queste
considerazioni, Prigogine e altri studiosi hanno cominciato a gettare un ponte
tra la fisica, la chimica, l'ecologia e le scienze sociali, per studiare tali
settori non separatamente, ma come sistemi tra loro interagenti. Per questa
ragione Prigogine è considerato uno dei pionieri della scienza della
complessità.
Il biofisico americano Harold Morowitz affrontò
esplicitamente la questione del flusso energetico e della produzione
dell'organizzazione biologica. L'ordine interno può essere prodotto da
gradienti di flussi di materia/energia attraverso i sistemi viventi. Le
strutture così prodotte aiutano non solo ad assorbire più energia attraverso il
sistema, ad allungare il suo tempo di ritenzione nel sistema, ma anche a
dissipare l'energia degradata nell'ambiente, pagando così il "debito di
entropia" di Schrödinger. I sistemi viventi sono quindi visti come un
esempio di un fenomeno più generale di strutture dissipative. “Una struttura
dissipativa si rinnova continuamente e mantiene un particolare regime dinamico,
una struttura spazio-temporale globalmente stabile”. Naturalmente, se si
verificano fenomeni di auto-organizzazione dipende dalle effettive condizioni
specifiche (iniziali e al limite) nonché dalle relazioni tra i componenti.
Considerare la cellula come una “struttura dissipativa”
termodinamica non era una riduzione della cellula alla fisica, come sottolineò
il fisico, biologo molecolare e storico della scienza britannico John Desmond
Bernal, ma piuttosto implicava una fisica della "complessità
organizzata" (in contrasto con l'ordine semplice o "complessità
disorganizzata"). Lo sviluppo di questa “nuova” fisica dei sistemi aperti
e delle strutture dissipative che sorgono in essi fu il compimento dello
sviluppo che Schrödinger aveva previsto. Le strutture dissipative nei sistemi
fisici, chimici e biologici sono fenomeni spiegati dalla termodinamica del non
equilibrio. I modelli spazio-temporali emergenti e auto-organizzati sono visti
anche nei sistemi biologici.
In effetti, i fenomeni di auto-organizzazione pervadono la
biologia. Tali fenomeni sono visti non solo nelle cellule e negli organismi, ma
anche negli ecosistemi, il che rafforza l'idea che sia necessaria una
prospettiva sistemica più ampia come parte della nuova fisica. Importanti per
tali fenomeni sono le dinamiche delle interazioni non lineari (dove le risposte
di un sistema possono essere molto più grandi dello stimolo) e dei cicli
autocatalitici (sequenze di reazioni chiuse su sé stesse e in cui è presente
una maggiore quantità di uno o più materiali di partenza). realizzati
attraverso i processi. Dato che i catalizzatori nei sistemi biologici sono
codificati nei geni del DNA, un punto da cui iniziare a definire la vita è
considerare i sistemi viventi come entità cicliche informate e autocatalitiche
che si sviluppano ed evolvono sotto i doppi dettami della seconda legge della
termodinamica e della selezione. Un tale approccio collega in modo non
riduttivo i fenomeni dei sistemi viventi con le leggi fondamentali della fisica
e della chimica. Il biologo americano Robert Rosen sosteneva che la complessità
non è la vita in sé, ma ciò che definiva "l'habitat della vita": “L'organizzazione
coinvolge intrinsecamente le funzioni e le loro interrelazioni”.
Origine (emergenza) della vita
Uno dei fenomeni emergenti più importanti è quello
dell'origine della vita. Il biologo cellulare Franklin Harold lo ha definito
come il problema scientifico più importante che oggi abbiamo di fronte. Il
filosofo della scienza britannico Michael Ruse ha affermato che è essenziale
inquadrare la ricerca sull'origine della vita nel darwinismo, poiché è una
condizione necessaria per una definizione della vita scientificamente e
filosoficamente adeguata, mentre Robert Rosen ha sostenuto che la ragione
per cui alla domanda "cos'è la vita?" è così difficile rispondere è
che vogliamo in realtà sapere molto di più di quello che è, vogliamo
sapere perché è: "Ci stiamo davvero chiedendo, in termini
fisici, perché uno specifico sistema materiale è un organismo e non
qualcos'altro". Per rispondere a questa domanda del perché dobbiamo
capire come potrebbe essere sorta la vita, continuando un filone di ricerca che
ha attraversato gran parte del ventesimo secolo.
Durante gli anni '20 del Novecento, Alexander Oparin e John
B. S. Haldane hanno proposto indipendentemente le prime ipotesi moderne su come
la vita potrebbe aver avuto origine sulla Terra. I presupposti chiave erano che
le condizioni geofisiche sulla terra primitiva erano molto diverse da quelle
presenti, e, cosa più importante, che non ci sarebbe stato ossigeno molecolare
nell'atmosfera (l'ossigeno si è sviluppato molto più tardi con la comparsa di
organismi fotosintetici). In questa atmosfera chimicamente riducente si sarebbe
sviluppato un “brodo” di molecole organiche sempre più complesse, da cui
potrebbero essere nati i precursori dei sistemi viventi. In effetti, questo tipo
di approccio può essere definito una visione incentrata sul metabolismo.
Un momento importante fu la dimostrazione che alcuni
amminoacidi potrebbero essere stati prodotti dall'azione di una scarica
elettrica attraverso una miscela di gas ritenuti presenti nell'atmosfera
primitiva. Si tratta del famoso esperimento di Stanley Miller e Harold Urey del
1953, che fu tuttavia contestato perché non dava conto del fatto che gli
amminoacidi trovati costituivano una miscela di enantiomeri levogiri e destrogiri,
mentre quelli delle proteine
viventi sono solamente levogiri. L’esperienza fu in ogni caso considerata un
altro possibile punto di partenza per lo sviluppo di sostanze costitutive degli
esseri viventi, ovvero le proteine, che sono polimeri di amminoacidi formate in
condizioni di alta temperatura. Questa visione di “prima le proteine” suggeriva
che la chimica che porta alla vita potrebbe essersi verificata in un ambiente
isolato, con una debole attività catalitica, che avrebbe facilitato la produzione
degli altri componenti molecolari necessari.
Con la comprensione della struttura del DNA, l'attenzione
si è spostata verso gli acidi nucleici, che potrebbero fungere da modelli per
la propria replicazione. Sebbene Dawkins pensasse che un acido nucleico,
formato per caso, sarebbe stato l'inizio della vita poiché si sarebbe
"auto replicato", molti approcci per arrivare agli acidi nucleici
implicano un ruolo per certe molecole abiotiche minerali di contribuire a
formare strutture che fungono da modelli di ordinamento e persino come
catalizzatori per la loro formazione.
Gli sviluppi degli studi biochimici, genetico-molecolari e
cellulari hanno confermato il ruolo fondamentale del DNA come macromolecola che
registra e trasmette le informazioni specifiche, ma hanno anche mostrato che la
vita non coincide con l'informazione contenuta nelle sequenze del DNA. La
scoperta che l'RNA può svolgere funzioni catalitiche ha dimostrato che
l'informazione genetica e il codice genetico sono nati successivamente nel mondo
vivente, ossia costituiscono un modo “trovato” per riprodurre più efficacemente
l'organizzazione biologica. Prima che il DNA diventasse la molecola che porta
l'informazione genetica esisteva il mondo dell'RNA, che racchiudeva in sé
entrambe le funzioni, di memoria e di catalizzatore di reazioni chimiche, che
successivamente si sarebbero separate.
Gli acidi nucleici, d’altra parte, non devono le loro
proprietà genetiche al fatto di essere polimeri o di potersi duplicare, bensì
alla trama di relazioni tra le loro proprietà e determinate funzioni
intracellulari che consente la riproduzione di queste funzioni. Anche per
quanto riguarda i geni, è entrata progressivamente in crisi la visione
tradizionale, che associava univocamente un gene a una data sequenza
nucleotidica e quindi a una data funzione: molti geni ritenuti essenziali
possono essere inattivati senza conseguenze, mentre per altri è possibile
trovare nuove funzioni. Ciò non significa che il DNA conti poco, ma soltanto
che il suo ruolo va compreso in un contesto evolutivo e funzionale.
Una visione alternativa, congeniale ad un approccio
termodinamico e sistemico sottolinea la necessità della presenza dei principali
fattori che distinguono le cellule dalle non cellule: metabolismo tramite cicli
autocatalitici di polimeri catalitici, replicazione e un involucro fisico
all'interno di una barriera chimica, come quella fornita dalla membrana
cellulare. Questo potrebbe essere definito un approccio “prima la
proto-cellula”. I vincoli chimici e le tendenze auto-organizzanti dei sistemi
chimici complessi sarebbero stati critici nel determinare
le proprietà dei primi esseri viventi. Con l'emergere delle prime entità che
potrebbero essere chiamate viventi sarebbe nata la selezione biologica o naturale, in cui la casualità gioca un ruolo molto maggiore.